1.-¿Qué es una disolución?
Las disoluciones son mezclas homogéneas de dos o más componentes, llamándose disolvente al que está en mayor proporción y soluto al que está en menor proporción
2.- ¿Como se puede expresar las concentraciones de las disoluciones?
Porcentaje en masa (m/m)
Porcentaje en volumen (V/V)
Porcentaje masa a volumen (m/V)
Partes por millón (ppm)
Formalidad (F)
Molaridad (M)
Molalidad (m)
Normalidad (N)
Fracción molar (X)
Porcentaje molar (X%)
3.- Mencione los tipos de soluciones que conoce:
Porcentaje en masa (m/m)
Porcentaje en volumen (V/V)
Porcentaje masa a volumen (m/V)
Partes por millón (ppm)
Formalidad (F)
Molaridad (M)
Molalidad (m)
Normalidad (N)
Fracción molar (X)
Porcentaje molar (X%)
3.- Mencione los tipos de soluciones que conoce:
- Gas en líquido.
- Líquido en líquido.
- Sólido en líquido.
- Gas en gas.
- Líquido en gas.
- Sólido en gas.
- Gas en sólido.
- Líquido en sólido.
- Sólido en sólido.
4.- ¿Qué nos dice la ecuación de los gases ideales?
El volumen de un gas depende de la presión, temperatura y numero de moles
5.- ¿Qué es el punto de ebullición?
El punto de ebullición de una solución es la temperatura a la cual su presión de vapor es igual a la presión externa.
5.-_Cuales son los tipos de propiedades coligativas:
- descenso de la presión de vapor del disolvente
- elevación ebulloscópica
- descenso crioscópico
- presión osmótica._
6.- ¿Qué son la propiedades coligativas?
son aquellas que dependen del número de partículas (moléculas, átomos o iones) disueltas en una cantidad fija de solvente
7.- ¿Que son las soluciones electroliticas?
Son aquellas en las que el soluto se encuentra disuelto en el solvente formando IONES
Son aquellas en las que el soluto se encuentra disuelto en el solvente formando IONES
8.- En que consiste la disminución de presión de vapor?
La presión de vapor de un disolvente desciende cuando se le añade un soluto no volátil. Cuanto más soluto añadimos, menor es la presión de vapor observada.
9.- En que consiste la elevación del punto de ebullición?
En una solución ideal, para llevar la solución a ebullición, debe aumentarse la temperatura. Por lo anterior, el punto de ebullición de la solución es más alto que el del solvente puro.
10.- En que consiste la disminución del punto de fusión?
El descenso crioscópico es un fenómeno que ocurre para todos los solutos, en cualquier tipo de disolución –incluso en las ideales- y no depende de ninguna interacción específica de tipo soluto-disolvente. En el punto de congelación, la fase sólida y la fase líquida tienen el mismo potencial químico, es decir, son energéticamente equivalentes.
11.- En que consiste la presión osmótica?
La tasa de paso del solvente desde la solución menos concentrada hacia la más concentrada es mayor que la velocidad en la dirección opuesta. Así hay un movimiento neto de las moléculas de solvente desde la solución menos concentrada hacia la más concentrada, este proceso se llama osmosis, Siempre, el movimiento neto del solvente es siempre hacia la solución con la concentración de solutos más alta.
Las leyes que regulan los valores de la presión osmótica para disoluciones muy diluidas (como las que se manejan en Biología) son análogas a las leyes de los gases.
12.- ¿Qué dice la ley de Raoult?
“a una temperatura constante, el descenso de la Presión de Vapor es proporcional a la concentración de soluto presente en la solución”.
13.-¿Cómo se clasifican las membranas?
- impermeables: no son atravesadas ni por solutos ni por el disolvente
- semipermeables: no permiten el paso de solutos verdaderos, pero sí del agua
- dialíticas: son permeables al agua y solutos verdaderos, pero no a los solutos coloidales
- permeables: permiten el paso del disolvente y de solutos coloidales y verdaderos; sólo son impermeables a las dispersiones.
14.-¿Cuáles son las disoluciones isotónicas?
son aquéllas que manifiestan la
misma presión osmótica que la disolución de referencia
misma presión osmótica que la disolución de referencia
15.- ¿Cuáles son los tipos de transporte a través de la membrana?
Transporte activo y transporte pasivo
16.- Menciona algunos ejemplos del transporte pasivo
Osmosis, difusión simple, difusión facilitada
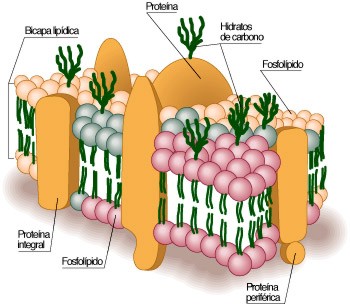
17.- ¿Qué tipo de proteínas se encuentran en la membrana plasmática?
menciones sus características
*Integrales que tiene uno o mas segmentos que atraciezan la bi capa lipidica
*Perifericas son proteinas que no tienen segmentos incluidos en la bicapa, sinembargo interacciona con la cabezas polares o con las proteinas integrales.
18.- Mencione las partes de un fosfolipido
cabeza polar (hidrofilica) y dos colas no polares (hidrofobicas), esto los convierte en "anfipaticos".
19._¿Cual es el principio del transporte activo?
Es cuando las moleculas van encontra de una gradiente de concentracion y requere un gasto energatico de ATP.
20.- En el trasporte pasivo (difusion facilitada) cual es el mediador que promueve el paso de las moleculas:
Suele ser una proteina integral de membrana. cuya conformación determina un canal interior, y por el cual un determinado sustrato puede alcanzar el interior, sin gasto de energía.
21.- Defina el concepto de "simporte"
el transporte simultáneo de dos sustratos en la misma dirección, por un mismo transportador sencillo.
22._ ¿Cuales son las bombas mas comunes en la mabrana plsmatica que requieren transporte activo?
Bomba de sodio/potasio.
Bomba de Calcio
23.- ¿Qué es el soluto y qué es el disolvente en una disolución?
En una disolución de una sustancia en otra, la sustancia disuelta se denomina soluto. La sustancia donde se disuelve el soluto se denomina disolvente. Cuando la cantidad relativa de una sustancia en una disolución es mucho mayor que la de otra, la sustancia presente en mayor cantidad se considera generalmente como disolvente.
24. ¿Define el potencial de membrana y porqué se produce?
El potencial de membrana se refiere a la diferencia de cargas eléctricas a través de la membrana plasmática. Fuera de la membrana tiene carga positiva debido a los iones Na+ y Ca2+ en grandes concentraciones y por dentro de la membrana la carga es negativa debido a grupos cargados negativamente en el citoplasma.
El potencial de membrana se genera, porque existe una distribución desigual de iones a través de la misma, y porque la membrana tiene permeabilidad selectiva para las especies iónicas presentes.
Esto significa que existe un gradiente de concentración para las especies iónicas mayoritarias presentes.
Si las membranas biológicas fueran simplemente una membrana bicapa fosfolipidica, totalmente impermeable a los iones, no se generaría un potencial de membrana, aunque existieran gradientes electroquímicos importantes a través de ella.
25.- ¿Qué es la transmisión sináptica?
se refiere a la propagación de los impulsos nerviosos de una célula hacia otra.
26.-¿Cómo se lleva a cabo la transmisión sináptica?
Los impulsos nerviosos son transmitidos en la brecha sináptica por la liberación de químicos denominados neurotransmisores. Cuando el impulso nervioso, o el potencial de acción llega al final del axón pre-sináptico, las moléculas del neurotransmisor son liberadas hacia la brecha sináptica. Los neurotransmisores son un grupo diverso de compuestos químicos, desde aminas simples como la dopamina y amino ácidos tales como el acido gamma-amino butírico (GABA), hasta polipéptidos como las encefalinas. Los mecanismos por los cuales se produce una respuesta en ambas neuronas pre-sinápticas y post-sinápticas son tan diversos como los mecanismos usados por el factor de crecimiento y los receptores de citocinas.
27.- ¿Qué son las membranas?
Son estructuras delgadas y flexibles que recubren un órgano o tapizan una cavidad. Función: de protección, secreción, absorción, nutrición y defensa.
28.- ¿Qué es un electrodo?
Extremo de un conductor en contacto con un medio, al que lleva o del que recibe una corriente eléctrica.
29.- ¿Qué es electroforesis y cómo se lleva a cabo?
Es una técnica para la separación de moléculas según la movilidad de estas en un campo eléctrico. La separación puede realizarse sobre la superficie hidratada de un soporte sólido (p. ej., electroforesis en papel o en acetato de celulosa), o bien a través de una matriz porosa (electroforesis en gel), o bien en disolución (electroforesis libre). Dependiendo de la técnica que se use, la separación obedece en distinta medida a la carga eléctrica de las moléculas y a su masa.
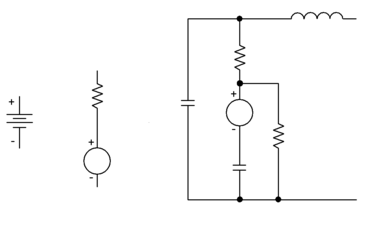
30.-¿En qué consiste la estructura de una pila?
La estructura fundamental de una pila consiste en dos electrodos, metálicos en muchos casos, introducidos en una disolución conductora de la electricidad o electrolito

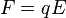





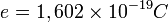 es la carga del electrón.
es la carga del electrón.